来源:生物探索
导语:生老病死似乎是每一个生命体都逃脱不出的命运轮回,但并不妨碍人们对长生不老的幻想和渴求。关于衰老究竟是什么,许多假说给出了它们自己的解释,但一个全面而统一的衰老理论仍有待形成。这里,西北大学的研究人员提出了一种全新的衰老驱动机制——细胞中长短基因活性的失衡将带来衰老,而改变这种失衡,则能减缓、甚至逆转衰老的进程。
美人迟暮、英雄白头都是令人扼腕叹息的场面,不仅因为这是一种悲剧,更因为其发生的必然性。在《34 岁不仅是“职场赛点”,也是“断崖式衰老”的开端,60 岁和 78 岁更是大坎!》一文中,我们曾描述了衰老带来的血浆蛋白组变化,有一些蛋白质在青年到中年过渡阶段断崖式下跌,有一些在老年阶段却指数式增长,这些蛋白波峰与疾病出现都与衰老基因的表达相关。
在 2013 年发表于 Cell 的综述性文章 "The Hallmarks of Aging" 中,作者则提出了衰老的 9 大特征:1)基因不稳定性(Genomic Instability);2)端粒缩短(Telomere Attrition);3)表观遗传学改变(Epigenetic Alterations);4)蛋白稳态丧失(loss of proteostasis);5)营养感应失调(deregulated nutrient sensing);6)线粒体功能异常(mitochondrial dysfunction);7)细胞衰老(cellular senescence);8)干细胞耗竭(stem cell exhaustion);9)细胞间信息交换改变(altered intercellular communication)。
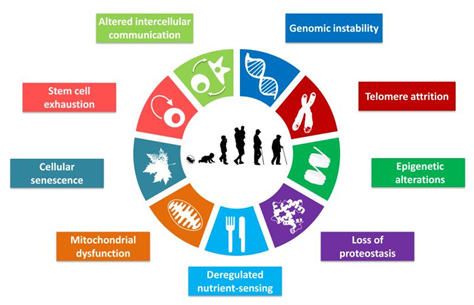
图1:衰老的特征(图源:[1])
但,又是什么“启动”了衰老的进程呢?
众说纷纭
目前,有许多学说都提出了关于衰老为什么会发生的解释。体细胞突变学说认为,在生物体的一生中,外界因素诱发的自发的突变破坏了细胞的基因和染色体,当突变积累到一定程度,将导致细胞功能下降以及死亡,然而目前已证明的基因突变率不足以支撑这一学说。
Denham Harman 在 1956 年提出的自由基学说认为,细胞正常带血过程中会产生有害的自由基,自由基不断积累将会引起 DNA 损伤导致突变,诱发肿瘤形成,但这一学说尚无实验依据,也未能解释老年人自由基清除能力下降的原因。
生物分子自然交联学说认为,生物衰老是由于各种生物大分子中化学活泼基团相互作用导致生物分子缓慢交联,使得生物体从一个不稳定的化学体系趋向化学活性的稳定,原有分子结构随着活泼基团的不断消耗而结构逐渐改变,使得生物组织逐渐出现衰老现象。但同样,该学说没有提出分子交联导致衰老的直接依据,也未能建立衰老的实验模型。
衰老的免疫学说分为两种观点,一者认为免疫功能的衰退是造成机体衰老的原因,一者认为自身免疫决定了衰老的发生。虽然以往的研究证实机体在衰老的过程中伴随着免疫功能的变化,但也有证据表明,免疫系统不是生存期的决定因素,这一学说也尚未解释免疫系统随着年龄增长而退化的原因。
端粒学说认为,端粒这一结构会在细胞每次分裂的过程中丢失一段序列,当端粒长度缩短到一定程度,细胞就会停止分裂,走向衰老和死亡。然而却存在着个体寿命及不同组织器官预期寿命与端粒长度、端粒酶活性不匹配的情况。
除此之外,美国的遗传学家 David Sinclair 更是语出惊人,直言“衰老是一种病”,换句话说也就是有可能通过药物来“治愈”衰老。他认为,衰老是由于表观遗传学的信息随着时间的推移而发生了丢失,细胞逐渐失去了在正确时间打开正确基因的能力,而人们只需要改变几个简单的习惯,就能够更健康长久地生活。
失衡的基因
不论 Sinclair 的观点是否正确,这一次,西北大学的研究人员则在人类、小鼠、大鼠和鳉鱼身上收集到的各种组织的数据中发现,可以从不同长度基因活性失衡这一角度解释衰老过程中发生的诸多分子水平的变化,而这种变化普遍存在于多种动物(包括人类)的多种组织(血液、肌肉、骨骼,以及肝脏、心脏、肠道、大脑、肺等器官)中。
研究结果以 Aging is associated with a systemic length-associated transcriptome imbalance 为题于 12 月 9 日发表于 Nature Aging。

图2:研究成果(图源:[3])
研究人员发现,年龄的增长以一种微妙但全局的方式影响着转录组,转录组的这种变化与基因调控的经典例子相比,变化的幅度较小,而且如果仅考虑单个基因的表达,将不容易注意到这种变化。令人吃惊的是这种变化在不同组织和不同动物中均有存在。
转录组的变化意味着基因活性的改变,与年龄增长相关的这种变化具体表现为活性向短基因的方向偏移。另一方面的事实是,基因的长度将决定其表达的蛋白质的大小,长基因将产生较大的蛋白质,短基因则产生较小的蛋白质。研究人员发现,较长的基因与较长的寿命相关,而较短的基因与较短的寿命相关。“一些短基因在生存方面具有短期优势,不过可能代价是牺牲最终的寿命。”这项研究的第一作者、博士后学者 Thomas Stoeger 说。
研究的通讯作者、西北大学复杂系统研究所 McCormick 工程学院化学与生物工程教授 Luis A. Nunes Amaral 表示:“想象服务员需要平衡手中的托盘。如果托盘里面的东西不平衡,那么服务员需要付出额外的努力来对抗这种不平衡。当生物体中的长短基因的活性平衡发生改变,就好比托盘离平衡越来越远。这些细微的变化看似没什么大不了的,但却需要细胞和生物体付出更多的努力去保持平衡。这就是基因的不平衡导致的衰老。”

图3:基因的失衡(图源:Youtube)
研究人员还考察了国家老龄化研究所(National Institute on Aging,NIA)在老龄化干预测试计划中提出的 11 种抗衰老干预措施,这些措施对延长寿命有很强的支持。结果表明,其中 7 种干预能够扭转这种与基因长度关联的转录组失衡。研究人员认为,这将为开发逆转或延缓衰老的疗法开辟新的途径。
Amaral 和 Stoeger 表示,目前治疗疾病的疗法就好比用泰诺来退烧,只是针对衰老的症状,而不是治疗引起发烧的疾病本身。Amaral 说:“发烧的原因有很多,它可能是由感染引起的,需要抗生素,或者是由阑尾炎引起的,需要手术。现在也是同样的问题,衰老是因为基因活性失衡。如果你能帮助纠正这种不平衡,那么你就能解决下游的后果。”
撰文:风立宵
排版:木子久
End
参考资料:
[1] López-Otín C, Blasco MA, Partridge L, et al. The hallmarks of aging. Cell. 2013 Jun 6;153(6):1194-217. doi: 10.1016/j.cell.2013.05.039. PMID: 23746838; PMCID: PMC3836174.
[2] https://www.bbc.com/zhongwen/simp/science-58884389
[3] Stoeger, T., Grant, R.A., McQuattie-Pimentel, A.C. et al. Aging is associated with a systemic length-associated transcriptome imbalance. Nat Aging 2, 1191–1206 (2022). https://doi.org/10.1038/s43587-022-00317-6






