
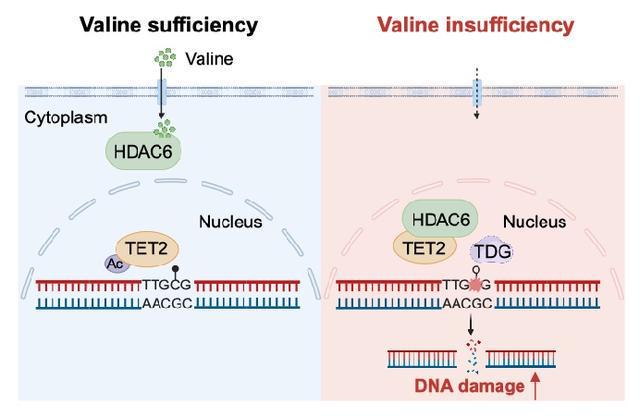
缬氨酸,作为一种必需的支链氨基酸,在蛋白质合成、神经行为、白血病进展中发挥着重要的作用。然而,细胞感应缬氨酸的机制与功能尚不清楚。为系统性鉴定缬氨酸的结合蛋白,研究团队通过质谱技术,筛选得到缬氨酸结合蛋白去乙酰化酶 HDAC6,显示出与缬氨酸更强的结合能力。研究团队进一步发现,有别于灵长类(人和猴子)的 HDAC6,鼠的 HDAC6 并不能与缬氨酸发生结合。这一发现揭示了不同物种在缬氨酸感应中的差异性,提示了物种进化在氨基酸感应中的重要作用。研究团队还通过诸多实验发现,细胞内缬氨酸匮乏能促进 DNA 损伤。由此,研究团队发现了全新的缬氨酸感应器,阐明了缬氨酸限制诱导 DNA 损伤的分子机制。
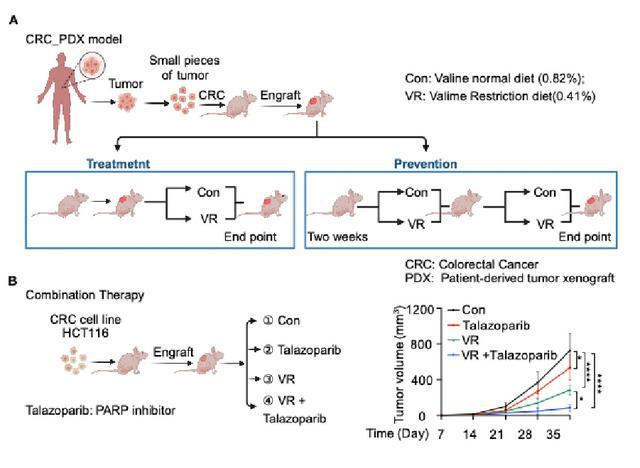
饮食限制或者靶向氨基酸代谢和感应,已成为延长寿命和癌症等多种疾病治疗的辅助策略。研究团队进而研究发现,在结直肠癌异种移植瘤和预防组、治疗组病人来源的异种移植肿瘤模型中,适宜的缬氨酸限制饮食(质量比为 0.41% 缬氨酸)可显著抑制肿瘤生长,同时产生的副作用较小。此外,缬氨酸限制性饮食和 DNA 修复酶抑制剂 talazoparib(他拉唑帕利)联合治疗显著增强抗肿瘤效果,这为该疗法通过诱导 DNA 损伤治疗癌症提供了有力的证据。
同济大学为论文的第一完成单位,王平教授为论文的唯一通讯作者,同济大学医学院金佳丽、孟通、俞媛媛和中国科学院分子细胞科学卓越创新中心吴树恒为该论文共同第一作者。该研究得到了同济大学江赐忠教授、中国科学院分子细胞科学卓越创新中心吴薇研究员、耶鲁大学吴殿青教授、同济大学医学院袁健教授、同济大学薛剑煌教授/王子昕、华东师范大学陈益华教授和沈阳药科大学曹昊教授等团队的合作和支持。本项研究获得了国家自然科学基金委国际合作项目、重点项目以及科技部国家重点研发计划等项目的资助。
团队长期深耕肿瘤微环境的基础研究和转化研究,致力于通过持续科研攻关找寻到攻击肿瘤细胞的分子机制,以期为肿瘤诊疗带来新思路和新策略。
王平说,这两项研究工作,涉及到多个领域,有幸得到了国内外同行在技术体系、专业背景等方面给予的支持。他感谢学校和附属第十人民医院医学科创中心在团队建设、科研设备平台等方面的有力支撑。
“我希望带领团队继续在肿瘤微环境研究领域深入探索,努力获得更多重要科学发现,为肿瘤等疾病诊疗带来新的启示和路径。”王平教授说。







